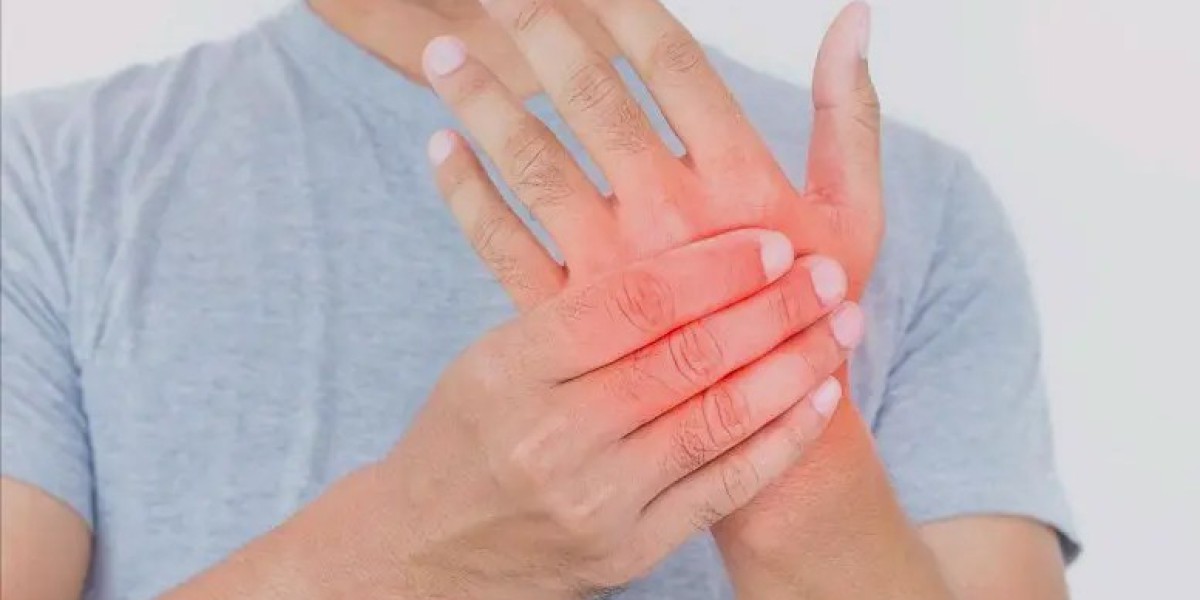
化疗引发的神经痛可能源自免疫细胞的应激反应,而非直接损伤神经。阻断这一反应或能帮助患者免受治疗中最具破坏性的副作用之一。
化疗可能通过激活免疫细胞内部的应激反应(而非直接损伤神经),引发炎症并导致神经损伤。这一发现或许能解释为何众多癌症患者在治疗期间出现剧烈疼痛。
由威尔·康奈尔医学院和维克森林大学医学院的研究人员共同完成的一项新研究表明,化疗可能触发免疫细胞内部的应激反应,从而导致炎症与神经损伤。化疗引起的周围神经病变(CIPN)影响高达半数的化疗患者,常导致手脚刺痛、麻木和疼痛。由于缺乏有效疗法,部分患者不得不减少甚至完全停止化疗。这项发表于《科学·转化医学》的临床前研究,为预防或管理 CIPN 提供了新思路,并可能帮助识别高风险患者。
“我们发现了一种特异性映射于免疫细胞(而非神经元)的分子机制,” 共同资深作者、威尔·康奈尔医学院妇产科感染与免疫学威廉·J·莱杰杰出副教授胡安·库维略斯-鲁伊斯(Juan Cubillos-Ruiz)博士表示:“这有力证明化疗诱导的神经病变不仅是神经问题,更是一种由细胞应激反应驱动的免疫介导性炎症过程。” 该研究由维克森林大学医学院麻醉学教授 E·阿方索·罗梅罗-桑多瓦尔(E. Alfonso Romero-Sandoval)博士共同领导。
在早期研究中,库维略斯-鲁伊斯博士团队发现了一条名为 IRE1α-XBP1 的应激反应通路。该通路在免疫细胞内充当分子“警报系统”,当细胞承受压力时会被激活。先前实验表明,这一系统能在小鼠模型中加剧术后及炎症期间的疼痛。
为探究其在化疗相关神经损伤中的作用,研究人员采用了一种能高度模拟癌症患者症状的小鼠模型。他们发现,常用化疗药物紫杉醇会导致免疫细胞产生大量活性氧分子,使细胞处于应激状态,进而激活 IRE1α,促使免疫细胞进入高炎症模式。
一旦被激活,这些免疫细胞会迁移至背根神经节(连接肢体与脊髓的感觉神经集群),并释放炎症信号损伤周围神经,最终引发疼痛、对寒冷过度敏感及神经纤维缺失等典型 CIPN 症状。
当研究人员从遗传学层面关闭免疫细胞中的 IRE1α 后,小鼠的炎症反应得到抑制,CIPN 样症状显著减轻。团队还测试了一种特异性抑制 IRE1α 的药物(该药已作为癌症疗法进入Ⅰ期临床试验)。联合使用紫杉醇与该抑制剂的小鼠,疼痛相关行为减少,神经组织保持更健康状态。
库维略斯-鲁伊斯博士(同时兼任威尔·康奈尔桑德拉与爱德华迈耶癌症中心癌症生物学项目共同负责人)指出:“我们的研究提示,药物靶向 IRE1α 或可减轻紫杉烷类药物引发的神经病变,帮助患者在不遭受神经损伤副作用的前提下完成化疗。” 由于 IRE1α 抑制剂已在晚期实体瘤患者中开展试验(该通路过度活化已知会促进癌症生长和耐药),研究人员认为此类药物可能同时帮助患者预防化疗神经损伤。库维略斯-鲁伊斯博士表示,这种双重获益 “有望显著提升癌症治疗效果与患者生活质量”。
为验证实验室发现与临床的关联,研究团队开展了一项小型先导研究,纳入接受紫杉醇治疗的妇科癌症患者。化疗周期前后采集的血样显示,后期出现严重 CIPN 的患者,其循环免疫细胞中的 IRE1α-XBP1 通路活性在症状显现前已显著升高。这表明未来或可通过血液检测识别神经病变高危患者,使医生能在神经损伤发生前采取预防性措施(包括潜在使用 IRE1α 抑制剂)。
核心摘要:
- 关键机制:化疗通过激活免疫细胞内的 IRE1α-XBP1 应激通路引发炎症性神经损伤。
- 干预突破:抑制 IRE1α 可显著减轻动物模型的神经病变症状,现有抑制剂已进入癌症临床试验。
- 临床转化:患者免疫细胞中该通路的活性或可作为预测神经病变的血液标志物。
- 双重获益:靶向该通路既可能保护神经,又有助增强抗癌疗效。
研究资助:该研究获美国国立卫生研究院下属国家癌症研究所、国家神经疾病与脑卒中研究所以及美国国防部的支持。
编辑说明:文章编译自《科学·转化医学》期刊,旨在传递前沿医学进展。所有治疗方案需在临床医生指导下进行。
参考文献:《白细胞内源性内质网应激反应导致化疗诱导的周围神经病变》,作者:Miriam M. Fonseca、Juan R. Cubillos-Ruiz 和 E. Alfonso Romero-Sandoval 等,2025年10月29日发表于《科学·转化医学》。
DOI:10.1126/scitranslmed.ady5288